Complexe activé

Dans l’ouvrage de 1896* apparaît également une explication de la cause des vitesses des réactions : « Le fait qu’une réaction a besoin d’un certain temps pour s’accomplir démontre qu’à côté de la cause qui la produit, et que nous nommerons la force impulsive ou l’affinité, il y a une force retardatrice qui entre en jeu. » Parmi les facteurs explicatifs de cette force retardatrice, outre la probabilité de rencontre des molécules (autrement dit les chocs efficaces), on trouve l’orientation des molécules, la vitesse de déplacement des molécules dans le solvant et le déplacement (l’échange) d’atomes. Certains corps ou mélanges de corps peuvent ainsi exister dans un « état d’équilibre apparent ».
[…]
À la fin du XIXe siècle, les lois de vitesse ainsi que les notions d’ordre de réaction et de molécularité ont été établies sur des bases expérimentales et admises par la communauté des chimistes. Van’t Hoff puis Arrhenius, qui ont adopté l’hypothèse atomique, commencent à modéliser à l’échelle moléculaire en considérant que la vitesse d’une réaction est liée aux collisions ou chocs entre les molécules. Lors de l’étude de l’influence de la température sur la vitesse d’une réaction, Arrhenius introduit dans le processus de réaction un stade intermédiaire, l’état d’activation, dans lequel certaines molécules, au prix d’une certaine absorption d’énergie, se trouvent dans un état exceptionnel différent de l’état moyen des molécules normales.
* Van’t Hoff J.H. (1896), Leçons de chimie physique professées à l’Université de Berlin, Traduction française de M. Corvisy, Hermann, Paris, 1898.
Alain DUMON. La naissance des concepts de la cinétique chimique au XIXe siècle. L’actualité chimique.
https://www.cnrs.fr/cnrs-images/chimieaulycee/AUTRES/scientifiques/savants.htm
Jacobus Henricus VAN’T HOFF. Chimiste hollandais (1852-1911) – Prix Nobel de chimie en 1901. Premier Prix Nobel de chimie de l’Histoire, Van’t Hoff se fait remarquer dès ses 22 ans en publiant un mémoire expliquant la relation entre la structure des composés organiques et leur activité optique. Il propose également la géométrie tétraédrique du méthane et des composés apparentés. Il est ainsi, avec Achille Le Bel, un des principaux fondateurs de la stéréochimie. Ses études sur les relations entre température et vitesse de réaction poseront par la suite les bases de la cinétique chimique. Van’t Hoff reçoit son Prix Nobel pour la découverte des lois de la dynamique chimique et de la pression osmotique dans les solutions.
Svante August ARRHENIUS. Chimiste suédois (1859-1927) – Prix Nobel de chimie en 1903. Ses travaux sur la dissociation électrolytique constituent les bases de la chimie physique et de l’électrochimie. Il prouve que dans les solutions électrolytiques, les composés chimiques dissous sont dissociés en ions, même en l’absence de courant traversant la solution. Il démontre l’influence de la température et de la concentration des espèces activées sur la vitesse d’une réaction. La loi qui porte son nom met ainsi en évidence la variation de la constante d’équilibre d’une réaction chimique en fonction de la température.

—————————————–
Tous les documents nécessaires sont téléchargeables à l’adresse DOCS (dossier cinetique (3)).
———————————-
On étudie ici les facteurs, essentiellement la température et la concentration pour les réactions en solution, qui influencent la vitesse des réactions chimiques.
Une partie expérimentale qualitative permet d’observer les effets :
[observations.pdf].
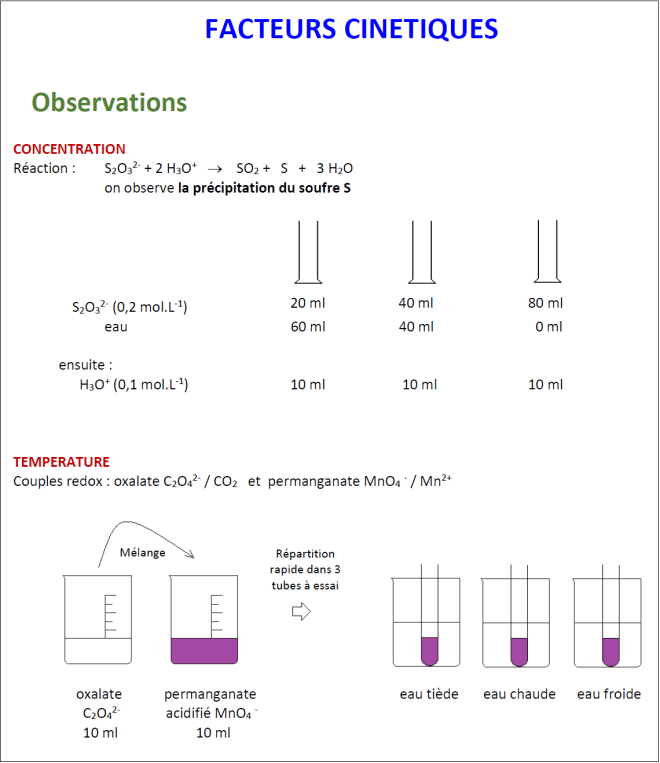
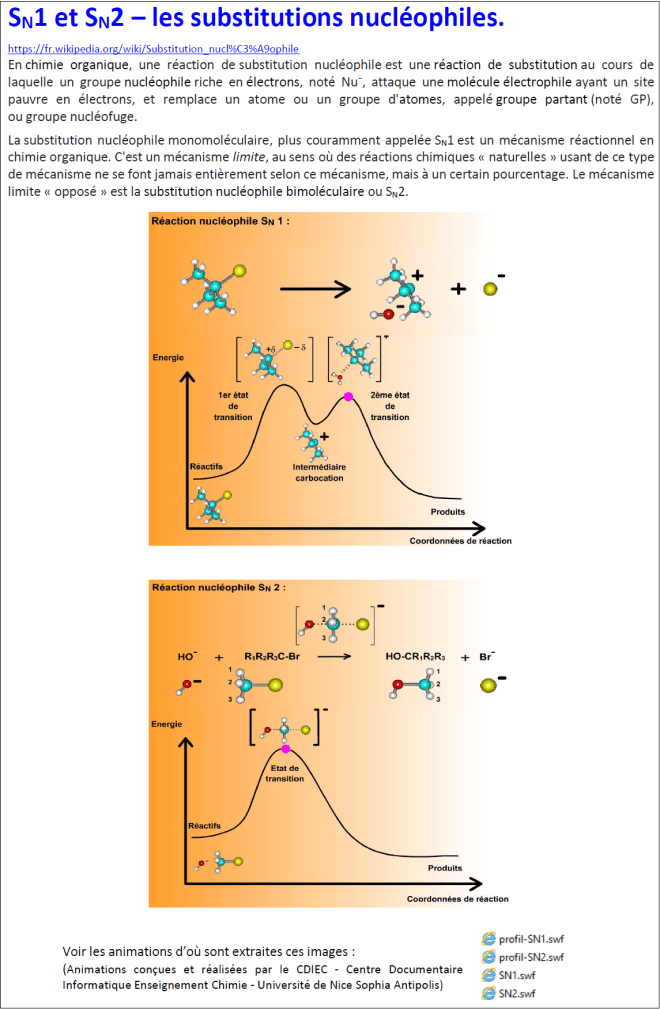
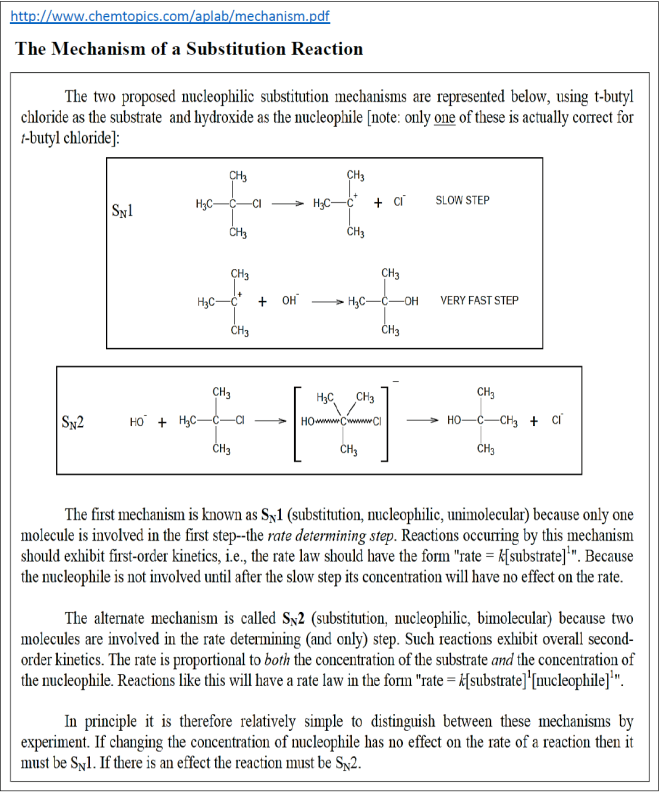
Une construction théorique est abordée, avec notamment les notions de complexe activé, de choc efficace et de profil réactionnel : [interpretations.pdf]. Les documents [SN.pdf] et [mechanism.pdf] ainsi que des animations et diaporamas sont exploitables pour élaborer l’interprétation du rôle des facteurs cinétiques.

—————————————–
Tous les documents nécessaires sont téléchargeables à l’adresse DOCS (dossier cinetique (3)).

———————————————————-