« Energies » de liaison et « énergie » de réaction
Animation de la dissociation d’une molécule diatomique AB en deux atomes A et B
https://fr.wikipedia.org/wiki/%C3%89nergie_de_dissociation_d%27une_liaison
En chimie, l’énergie de dissociation d’une liaison (D0) réfère à l’une des mesures de l’énergie d’une liaison chimique. Elle correspond au changement d’enthalpie lors d’un clivage homolytique avec des réactifs et des produits de la réaction d’homolyse* à 0 K (zéro absolu). D’ailleurs, l’énergie de dissociation d’une liaison est parfois appelée l’enthalpie de dissociation d’une liaison. Cependant, ces termes ne sont pas strictement équivalents car l’enthalpie de dissociation d’une liaison réfère à la réaction de dissociation dans les conditions normales de température et de pression. Cela amène une différence d’environ 1,5 kilocalorie par mole (kcal/mol), ou 6 kJ/mol, dans le cas d’une liaison hydrogène dans une grande molécule organique.
* rupture homolytique ou clivage homolytique est la rupture d’une liaison covalente en deux fragments ; chacun retenant l’un des deux électrons du doublet d’électrons liants.
Exemple :
L’énergie de dissociation de l’un des liens C–H de l’éthane (C2H6) est donnée par la réaction :
CH3CH2–H → CH3CH2· + H·
D0 = ΔH = 101,1 kcal/mol (423,0 kJ/mol).
Extrait
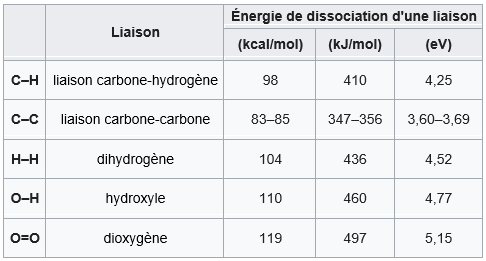
https://fr.wikipedia.org/wiki/%C3%89nergie_de_liaison_(chimie)
Elle [l’énergie de liaison] représente l’énergie requise pour briser une mole de molécules en atomes individuels. Par exemple, l’énergie de la liaison carbone-hydrogène dans le méthane, E(C–H), est l’enthalpie nécessaire pour casser une molécule de méthane en un atome de carbone et quatre atomes d’hydrogène, divisée par 4.
L’énergie de liaison ne doit pas être confondue avec l’énergie de dissociation de liaison, qui est, en dehors du cas particulier des molécules diatomiques, une quantité différente. L’énergie de liaison représente en fait la moyenne des énergies de dissociation des liaisons de même type d’une molécule. L’énergie de liaison est, en première approche, une propriété transférable, et l’enthalpie de formation peut typiquement être approchée en additionnant simplement les valeurs tabulées de l’énergie de toutes les liaisons d’une molécule, avec parfois une erreur de seulement quelques pourcents.
L’énergie de liaison ne doit pas être confondue avec l’énergie de dissociation de liaison, qui est, en dehors du cas particulier des molécules diatomiques, une quantité différente. L’énergie de liaison représente en fait la moyenne des énergies de dissociation des liaisons de même type d’une molécule.
——————————
Tous les documents indiqués sont téléchargeables à l’adresse DOCS (combustions 6)
—————————
On aborde ici la notion d’énergie de liaison et énergie de réaction (de façon très simplifiée par rapport aux subtilités thermodynamiques !).
[energie-liaison-reaction.pdf]
[methane.pdf]

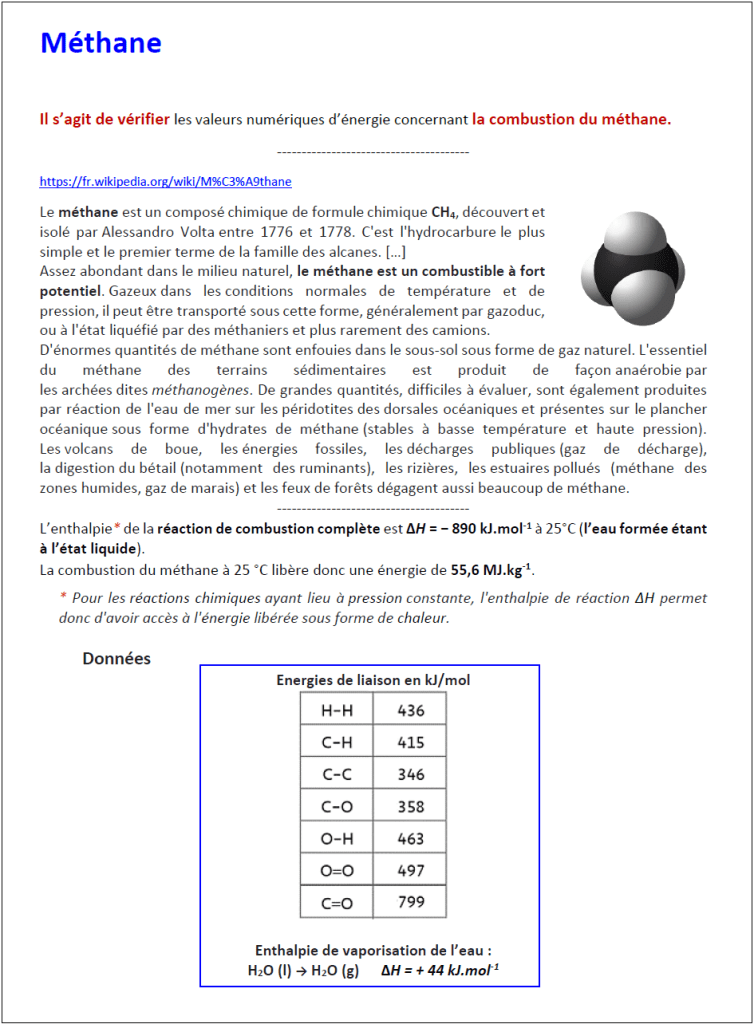
[methane-corrige.pptx]
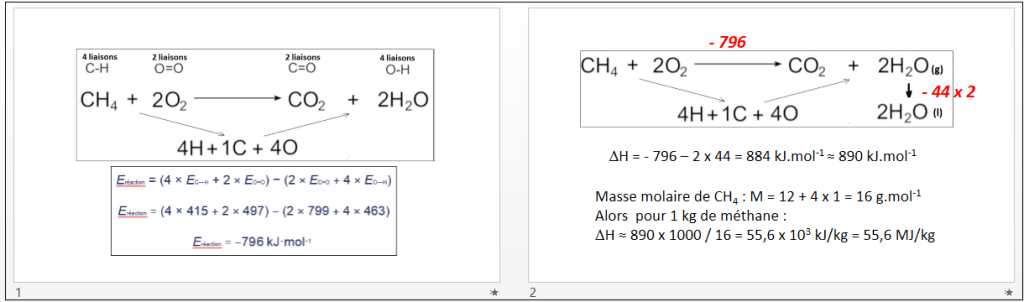
——————————
Tous les documents indiqués sont téléchargeables à l’adresse DOCS (combustions 6)

——————————————————————–